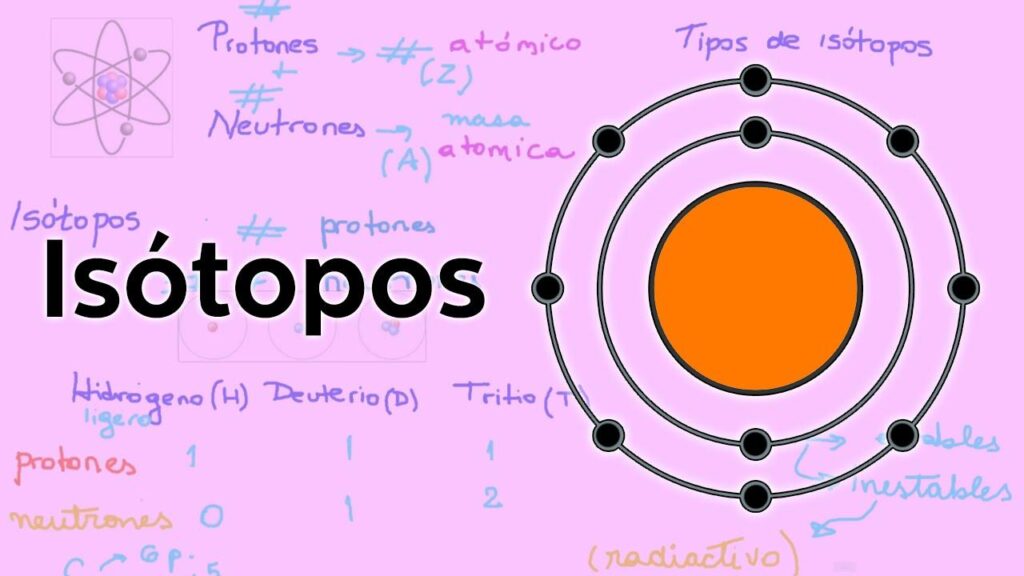
En este artículo abordaremos la interesante temática de los isótopos, explicando cómo surgen y cuáles son sus características principales. Los isótopos son átomos de un mismo elemento químico que varían en su número de neutrones, lo que les confiere propiedades y usos diferentes. ¡Acompáñanos en este fascinante recorrido por el mundo atómico!
El fascinante origen de los isotopos: la naturaleza de su formación.
¿Cuál es la partícula responsable de la creación de isótopos?
La partícula responsable de la creación de isótopos es el neutrón. Los átomos de un mismo elemento químico tienen el mismo número de protones en su núcleo, lo que define su número atómico. Sin embargo, pueden tener diferente cantidad de neutrones, lo que les da distinto tamaño y masa, pero con iguales propiedades químicas. A estos átomos se les llama isótopos. La creación de isótopos se produce por procesos como la radiactividad, el bombardeo de núcleos atómicos o mediante reacciones nucleares en laboratorios.
¿Cuál es la función y definición de los isótopos?
Los isótopos son átomos de un mismo elemento químico que tienen el mismo número de protones en el núcleo, pero difieren en la cantidad de neutrones. Esta diferencia en la cantidad de neutrones hace que los isótopos tengan masas diferentes, pero mantengan las mismas propiedades químicas y eléctricas.
La función de los isótopos es amplia y variada, ya que se utilizan en muchos campos de la ciencia y la tecnología. Por ejemplo, los isótopos radiactivos se utilizan en medicina para el diagnóstico y tratamiento de enfermedades, y también se usan en la datación geológica y arqueológica.
Por otro lado, los isótopos se utilizan en la agricultura para estudiar el movimiento de nutrientes en las plantas, en la industria alimentaria para determinar la procedencia de alimentos y bebidas, en la física nuclear para investigar las propiedades de los núcleos atómicos, entre otras aplicaciones.
En resumen, los isótopos son átomos de un mismo elemento con diferentes masas nucleares debido a la variación en la cantidad de neutrones. Tienen diversas aplicaciones en la ciencia y la tecnología, en campos como la medicina, la agricultura, la industria alimentaria y la física nuclear, entre otros.
¿Qué son los isotopos y cómo se forman?
Los **isótopos** son átomos de un mismo elemento químico que poseen la misma cantidad de protones en su núcleo, pero difieren en el número de neutrones. Esto significa que tienen el mismo número atómico, pero diferente número másico.
La formación de los isótopos se puede dar de manera natural o artificial. De manera natural, los isótopos se forman a través de procesos de desintegración radiactiva en los núcleos de los átomos. Estos procesos liberan energía y partículas subatómicas que pueden transformar el núcleo original en otro con características distintas.
Por otro lado, los isótopos también se pueden crear de manera artificial mediante reacciones nucleares inducidas, como la captura de neutrones por un núcleo, la irradiación de un blanco con protones, o la fusión de núcleos ligeros en un reactor nuclear. Estas técnicas son utilizadas en campos como la medicina, la investigación, la energía y la industria.
¿Cuáles son los procesos y fenómenos naturales que generan isotopos?
Los procesos y fenómenos naturales que generan isotopos son:
1. Decaimiento radiactivo: es el proceso por el cual un núcleo inestable emite partículas alfa, beta o gamma, para convertirse en un isótopo más estable.
2. Fisión nuclear: es el proceso en el que un núcleo pesado se divide en dos o más fragmentos más pequeños, liberando gran cantidad de energía y produciendo isótopos más ligeros.
3. Fusión nuclear: es el proceso en el que dos núcleos ligeros se combinan para formar uno más pesado, liberando una gran cantidad de energía y produciendo nuevos isótopos.
4. Captura de neutrones: es el proceso en el que un núcleo absorbe un neutrón para formar un isótopo más pesado.
5. Ciclo del agua: durante la evaporación, los isótopos más ligeros del agua se evaporan con mayor facilidad que los isotopos más pesados, lo que puede dar lugar a variaciones en la composición isotópica del agua en diferentes partes del mundo.
6. Reacciones químicas: algunos isotopos son producidos como productos secundarios en reacciones químicas, como la producción de radioisótopos en reactores nucleares.
En resumen, los procesos que generan isotopos son variados y ocurren naturalmente en la Tierra, siendo importantes para entender la historia geológica, climática y evolutiva de nuestro planeta y del universo en general.
¿Cómo se utilizan los isotopos en la industria y en la investigación científica?
Los isótopos se utilizan en diferentes aplicaciones en la industria y en la investigación científica.
En la industria, los isótopos se usan para una variedad de propósitos, desde la trazabilidad de materiales hasta la seguridad alimentaria. Uno de los usos más comunes de los isótopos es en la agricultura, donde se utilizan para estudiar el movimiento de nutrientes en el suelo y en las plantas. También se utilizan para la identificación de fugas en tuberías y en la industria petrolera para estudiar la producción de petróleo y gas.
En la investigación científica, los isótopos se utilizan para una amplia gama de aplicaciones, incluyendo datación radiométrica, estudios de metabolismo y diagnóstico médico. La datación radiométrica utiliza los isótopos para determinar la edad de las rocas y otros objetos geológicos. Los estudios de metabolismo utilizan los isótopos para rastrear la absorción, transporte y transformación de las moléculas en el cuerpo humano. Por último, los isótopos también se utilizan en técnicas de diagnóstico médico, como la tomografía por emisión de positrones (PET) y la espectrometría de masas.
En conclusión, los isótopos tienen una amplia gama de aplicaciones importantes en la industria y en la investigación científica.






